Тесты по химии 11 класс. Тема: “Органические и неорганические кислоты”
Правильный вариант ответа отмечен знаком +
1. Чем отличаются органические кислоты от неорганических?
+ у органических кислот имеются углерод-водородные связи
– неорганические кислоты никогда не имеют в своём составе углерод
– неорганические кислоты всегда имеют в своём составе углерод
– у неорганических кислот имеются углерод-водородные связи
2. Чем являются кислоты по теории электролитической диссоциации?
– донорами протонов
– акцепторами электронной пары
– молекулами или ионами, которые имеют неподелённую электронную пару
+ соединениями, которые образуются при растворении в воде из положительных ионов только ионы водорода H+
3. Чем являются кислоты по протолитической теории кислот и оснований Брёнстеда—Лоури?
– соединениями, которые образуются при растворении в воде из положительных ионов только ионы водорода H+
+ донорами протонов
– акцепторами электронной пары
– молекулами или ионами, которые имеют неподелённую электронную пару
4. Когда кислоты вступают в реакцию с основными или амфотерными оксидами, то при этом образуются:
– газ и малодиссоциирующее соединение
– сложные эфиры
+ соль и вода
– нет правильного ответа
5. Сложные эфиры образуются, когда кислота:
– взаимодействует с солями
– взаимодействуют с оксидами
– взаимодействует с металлами
+ вступает в реакцию этерификации
6. Какая из перечисленных кислот является кислородсодержащей?
– бромоводородная
+ серная
– сероводородная
– хлороводородная
7. Кислоту с максимальным числом оксогрупп OH при постоянной степени окисления элемента называют:
– метакислотой
– мегакислотой
+ ортокислотой
– нет правильного ответа
8. Каким способом нельзя получить кислоты?
– непосредственным соединением неметаллов с водородом
+ взаимодействием щелочных и щелочно-земельных металлов с водой
– взаимодействием кислотных оксидов с водой
– использованием окислительно-восстановительных процессов
9. Из перечисленных кислот, выберите ту, которая существует только в растворах.
+ H2CO3
– H2SO4
– HClO4
– H2SiO3
тест 10. Реакция нейтрализации наблюдается при взаимодействии кислот с:
– металлами
– солями
+ основаниями
– другими кислотами
11. При избытке основного оксида, соответствующего многокислотному основанию, образуется:
– кислая соль
-основная кислота
+ основная соль
-кислое основание
12. Если металл, который в ряду напряжений стоит после водорода, взаимодействует с кислотой-неокислителем, то:
– образуется соль металла и выделяется водород
– образуется кислота, соль металла и вода
– образуется кислотный остаток, соль металла и водород
+ реакция не идёт
13. Продукты восстановления кислоты окислителя не определяется:
– концентрацией кислоты
– активностью металла
– температурой
+ природой окислителя
14.Признак, определяющий число атомов водорода в молекуле, способных замещаться на металл, называется:
– летучесть
+ основность
– степень электролитической диссоциации
– стабильность
15. Из перечисленных ниже кислот, выберите нерастворимую:
+ пальмитиновая
– серная
– азотная
– уксусная
16. Молекулы уксусной кислоты способны без труда переходить в газообразное состояние. Это означает, что кислота:
– устойчивая
– неустойчивая
+ летучая
– нелетучая
17. По степени электролитической диссоциации, какая из перечисленных кислот характеризуется α→1?
– H2S
+ HNO3
– H2CO3
– CH3COOH
18. Выберите пару стабильных кислот.
– HCl и H2CO3
– H2SO3 и H2SiO3
+ H2SO4 и H3PO4
– H2SO3 и H2CO3
19. Каким способом получают органические кислоты?
+ окислением альдегидов и первичных спиртов
– взаимодействием кислотных оксидов и воды
– соединением неметаллов и водорода
– реакцией обмена между солями и кислотами
тест-20. Специфическим свойством неорганических кислот является:
– галогенирование
+ окислительно-восстановительные процессы
– замещение гидроксильных групп
– декарбоксилирование
21. Органические кислоты классифицируются по:
– по числу атомов водорода
– по наличию или отсутствию кислорода
– нет правильного ответа
+ по числу карбоксильных групп
22. Каким образом получают функциональные производные – ангидриды?
+ действием на кислоты водоотнимающих средств
– нагреванием солей аммония
– реакцией галогеналканов с цианидом щелочного металла
– нагревание кислоты со спиртом в присутствии серной кислоты
23. По какой теории ион аммония NH4+ является кислотой, а NH3 сопряжённым ей основанием?
– водородной теории Либиха
– теории электролитической диссоциации Аррениуса—Оствальда
– электронной теории Льюиса
+ протолитической теории Бренстеда–Лоури
24. У кислот имеются тривиальное и систематическое названия, например, уксусная – этановая. Какое систематическое название имеет валериановая кислота C4H9COOH?
– метановая
– пропановая
+ пентановая
– гексановая
25. На какой из приведённых ниже иллюстрация не изображена качественная реакция на карбоновые кислоты?

26. Для каких кислот характерны следующие признаки: бесцветные жидкости, резкий едкий запах, образование ассоциатов, в любых соотношениях смешиваются с водой?
+ для низших карбоновых кислот
– для высших карбоновых кислот
– для всех органических и неорганических кислот
– исключительно для неорганических кислот
27. На рисунке изображена кислота, которая обладает антисептическим свойствами и используется в пищевой промышленности. В природе она содержится клюкве, бруснике, малине и коре вишнёвого дерева. Эта кислота называется?
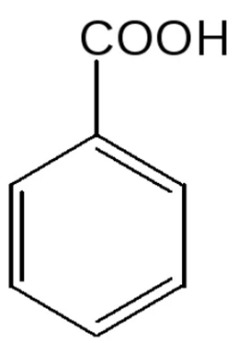
– муравьиная
– валерианова
– щавелевая
+ бензойная
28. Нитрилами называют:
– функциональные производные карбоновых кислот, в которых две ацильные группы соединены с одним атомом кислорода
+ функциональные производные карбоновых кислот, в молекулах которых карбоксильная группа замещена группой –СN
– производные неорганических кислот
– производные кислородсодержащих кислот, в которых гидроксильная группа замещена аминогруппой
тест_29. Насыщенные карбоновые кислоты устойчивы к действию сильных окислителей, исключением является кислота:
– лимонная
– щавелевая
+ муравьиная
– пропионовая

