Тесты по химии 11 класс. Тема: “Строение атома. Изотопы”
Правильный вариант ответа отмечен знаком +
1. Ниже изображена атомная модель химического элемента. Этот элемент:
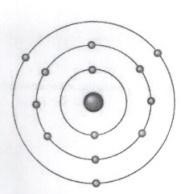
– магний
+ алюминий
– хлор
– сера
2. p-электронные облака имеют форму:
– сферы
+ восьмиобразной гантели
– листа клевера
– верного ответа нет
3. Количество электронов, протонов, нейтронов в атоме 40Ar составляет:
+ 18, 18, 22
– 15, 4, 20
– 16, 18, 36
– 22, 18, 40
4. Укажите название химического элемента, которому соответствует электронная конфигурация 1s22s22p63s23p2, а также формулу его водородного соединения:
– фосфор, PH3
+ кремний, SiH4
– фтор, HF
– сера, H2S
5. Показателям какого квантового числа соответствуют номера периодов?
– магнитного
+ главного
– орбитального
– спинового
6. Определите, чему равна разность Δ между значениями n0 и e– в атоме ¹⁹⁷Au:
– 118
– 40
– 79
+ 39
7. В ряду элементов B – N – F радиус атома:
– не изменяется
– увеличивается
+ уменьшается
– изменяется без закономерности
8. Какие из приведенных химических частиц являются изотопами?
+ 40Ar, 36Ar
– 39K, 20Ca
– 40Ca, 40Zr
– все три варианта верные
9. Количеством чего отличаются друг от друга изотопы одного и того же химического элемента?
– протонов
– атомов
+ нейтронов
– электронов
тест 10. Какое количество энергетических уровней свойственно элементу под №110?
– шесть
– четыре
– пять
+ семь
11. Схожесть атомов О2 с атомами S определяется:
– показателем атомной массы
– числом нейтронов
+ количеством электронов на внешнем энергетическом уровне
– коэффициентом электроотрицательности
12. Какому элементу соответствует состав 37p, 48n, 37е?
+ Rb
– Zn
– In
– Ge
13. Какой из элементов содержит одинаковое количество нейтронов и электронов?
– литий
– ион фтора
+ атом серы
– натрий
14. Какая электронная конфигурация не возможна?
– 1s2
+ 3f1
– 3d5
– все ответы верные
15. Заряд атома какого элемента равен +22?
– натрия
– фосфора
– кислорода
+ титана
16. Укажите формулу высшего оксида, которую образует химический элемент электронной конфигурации 1s22s22p63s23p3:
– ЭО2
+ Э2О5
– ЭО4
– Э2О
17. Какому иону свойственна двухэлектронная внешняя оболочка?
– С4+
+ Br5+
– Sn4+
– S2-
18. Способность атомов перемещать на себя общие пары электронов называется:
+ электроотрицательность
– изомерия
– аллотропия
– верного ответа нет
19. Атом какого элемента содержит в IV электронном слое 5 электронов?
– меди
+ мышьяка
– олова
– ванадия
тест-20. Какой элемент содержит 3 протона в атоме?
– бор
– фосфор
– алюминий
+ литий
21. Чему равно значение нейтронов в атоме ¹⁰⁸Ag?
– 47
– 108
+ 61
– 155
22. Что общего имеют атом Ne, анион F– и катион Na+?
– количество энергетических оболочек
+ число электронов
– массовое число
– показатель электроотрицательности
23. Значения 2,8,5 характерны размещению электронов на электронных слоях атома:
– Si
+ P
– S
– Mg
24. В каком периоде должно начаться заполнение энергетического 5f-подуровня?
+ седьмом
– четвёртом
– втором
– пятом
25. Изотопы химического элемента имеют:
– одинаковые значения нейтронов
– разные числа протонов
+ одинаковое размещение электронов по электронным слоям
– одинаковые массовые числа
26. Какой состав у аниона S?
+ 16 нейтронов
– 22 электрона
– 36 протонов
– 12 электронов
27. Какой из элементов относится к s-элементам?
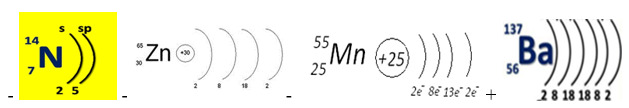
28. Атомы C и Si отличаются:
– числом валентности
+ количеством электронных слоёв
– принадлежностью к р-элементам
– значением электронов на последнем электронном слое
29. Равное количество нейтронов и электронов свойственно:
– натрию
– иону серы
– литию
+ атому серы
тест_30. При каком количестве электронов на d-подуровне он является наиболее устойчивым?
– 5
– 4
– 1
+ 10

