Тесты по химии 11 класс. Тема: “Виды химической связи”
Правильный вариант ответа отмечен знаком +
1. Укажите ряд, где приведены вещества только с ионной связью:
– SO3, P4, CaF2
– O2, ССl4, КСl
+ NaBr,Na2O, K2S
– H2S, Br2, K2S
2. Выберите вариант, в котором соединения расположены в порядке возрастания полярности связи:
– CH4-N2-NaCl-HF
– NaCl-N2-CH4-HF
+ N2-CH4-HF-NaCl
– HF-N2-NaCl-CH4
3. Чему равно количество совместных электронных пар между атомами брома в молекуле Br2?
+ одна
– две
– три
– четыре
4. Какое вещество является аллотропной модификацией O2?
– N2
– Si
+ O3
– C (алмаз)
5. Вставьте пропущенные слова: «Образование ионной связи возможно между атомами веществ, электроотрицательности которых …»
– незначительно отличаются
– совпадают
+ сильно отличаются
– практически совпадают
6. Неполярная ковалентная связь свойственна каждому из 2-х веществ:
– Ag, S
– графит, H2O
– Si, Zn
+ N2, алмаз
7. В процессе формирования ковалентной связи по обменному механизму два атома должны иметь соответственно:
+ неспаренный электрон и неспаренный электрон
– неспаренный электрон и неподеленную пару электронов
– свободную орбиталь и неподеленную пару электронов
– свободную орбиталь и неспаренный электрон
8. Какому элементу свойственна металлическая связь?
+ Ga
– As
– P
– I
9. Укажите разновидность классификации ковалентных связей, представленную на рисунке ниже:
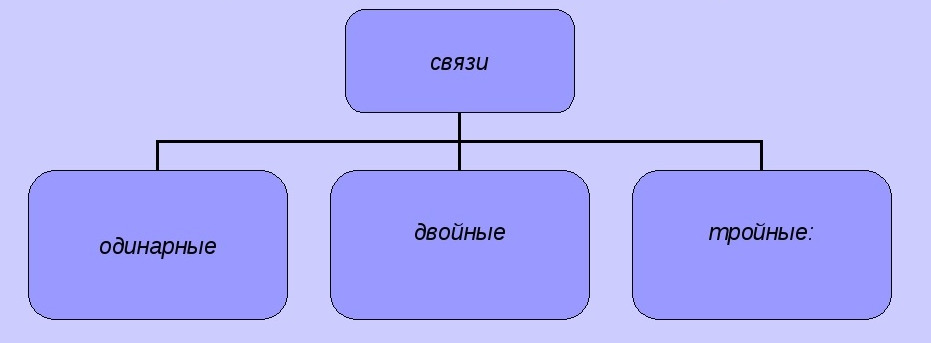
+ по количеству общих электронных пар
– по электроотрицательности
– по распределению электронной плотности
– по гибридизации атомных орбиталей
тест 10. Водородной связи характерно реализовываться:
– в молекуле Н2
– в молекуле Н2О
– между молекулами Н2
+ между молекулами Н2О
11. Наиболее электроотрицателен элемент:
– Cl
+ O
– Si
– Br
12. По принципу донорно-акцепторного механизма образована одна из связей в:
– молекуле Н2
+ ионе NH4+
– молекуле NH3
– молекуле H2O2
13. С увеличением заряда ядра атома электроотрицательность атома:
+ увеличивается в периоде, уменьшается в группе
– увеличивается в периоде, увеличивается в группе
– уменьшается в периоде, уменьшается в группе
– уменьшается в периоде, увеличивается в группе
14. Количество соединений с ионным типом связи в ряду K2S, PH3, NaBr, PCl3, CaBr2 равно:
+ три
– пять
– четыре
– две
15. К веществам с ионной связью относится:
– SiCl4
– H2S
– N2
+ CaI2
16. У какого соединения не ионный тип химической связи?
– NaCl
– CaI2
+ CO2
– KF
17. Как изменяется полярность связи в ряду HF→ H2S→ PH3→ SiH4?
– невозможно определить
+ убывает
– возрастает
– не меняется
18. Какая химическая связь у BaCl2?
+ металлическая
– ионная
– ковалентная неполярная
– ковалентная полярная
19. Полярная ковалентная связь формируется между атомами элементов, электроотрицательности которых:
– совпадают
+ незначительно отличаются
– очень сильно отличаются
– сильно отличаются
тест-20. Неполярную ковалентную связь имеет вещество:
– H2O
– O2
– F
+ CO2
21. Укажите два соединения, в каждом из которых есть ионные связи:
– NaCl, H₂O
– KNO₃, N₂
– Ba(OH)₂, NH₃
+ KOH, Na₂SO₄
22. Какой тип связи характерный для сероводорода (H2S)?
– металлический
– ковалентный неполярный
– ионный
+ ковалентный полярный
23. Наиболее полярная связь в молекуле:
+ CF₄
– F₂
– NF₃
– OF₂
24. В каком веществе имеется максимальное количество общих электронных пар между атомами?
– H2
+ N2
– HCl
– F2
25. Ковалентная неполярная связь характерна для вещества:
– CO2
– NH3
+ алмаза
– H2O
26. Какие типы химической связи следует вписать в местах пропусков на рисунке ниже?
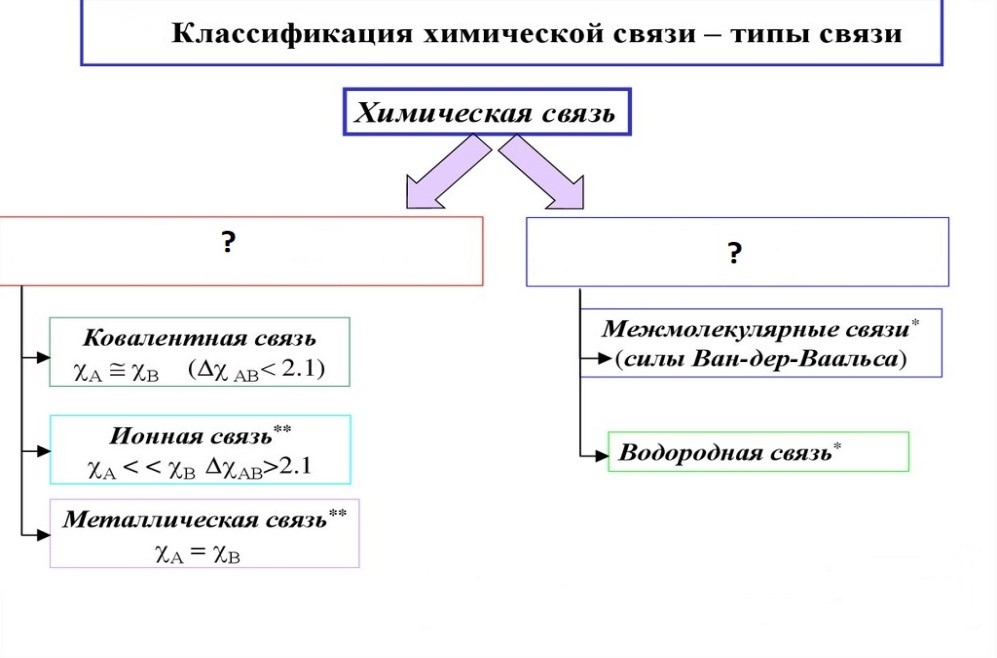
– в сложных веществах (слева), в простых веществах (справа)
+ сильные (слева), слабые (справа)
– простые (слева), сложные (справа)
– межмолекулярные (слева), молекулярные (справа)
27. Аллотропной модификацией углерода является:
– O3
+ алмаз
– S крист.
– SiO2
28. Вода имеет кристаллическую решетку:
– ионную
– атомную
+ молекулярную
– металлическую
29. Химическая связь имеет ионный характер между атомами химических элементов:
– азотом, озоном
– кремнием, хлором
+ натрием, кислородом
– фосфором, бромом
тест_30. Для какого вещества свойственны лишь ионные связи?
– Na2O2
– Ca(OH)2
+ CuSO4 X 5H2O
– NaCl

