Тесты по химии 9 класс. Тема: “Классификация химических реакций”
Правильный вариант ответа отмечен знаком +
1. Какому типу химических реакций соответствует взаимодействие BaCl2 с Rb2SO4?
– распада
+ обмена
– соединения
– замещения
2. Необратимой является реакция:
– дегидратации C3H7OH
– соединения SO2 с O2
+ разложения Al(OH)3
– гидрирования C2H4
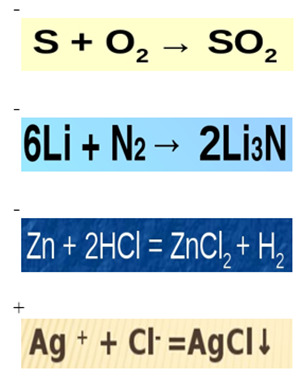
3. Выберите реакцию, которой свойственно в стандартных условиях протекать с наибольшей скоростью:
4. При каком условии происходит смещение химического равновесия реакции CO2+C <—–> 2CO-Q в сторону продуктов реакции?
– при снижении температуры
+ при увеличении температуры
– при уменьшении давления
– при повышении давления
5. Как изменится скорость химической реакции Н2 (г) + I2 (г) → 2HI(г) при повышении давления в 2 раза?
+ возрастёт в 4 раза
– уменьшится в 3 раза
– увеличится в 2 раза
– никак не изменится
6. Скорость взаимодействия раствора HCl будет максимальной с кусочком:
– Fe
+ Mg
– Zn
– Cu
7. Взаимодействие Zn с HCl относится к реакциям:
– разложения
– соединения
– обмена
+ замещения
8. Химическая реакция BaCl2+H2SO4=BaSO4+2HCl относится к реакциям:
+ обмена
– распада
– замещения
– соединения
9. Какая из реакций относится к каталитическим?
– взаимодействия HCl с Na2CO3
+ синтеза NH3
– хлорирования CH4
– бромирования анилина (C₆H₅NH₂)
тест 10. Какого цвета будет осадок в результате обмена между FeCl2 и NaOH?
– коричневый
– малиновый
+ зелёный
– фиолетовый
11. Гетерогенной обменной реакцией является реакция:
– NaOH + HCl = NaCl + Н2О
+ CuS + H2SO4 = CuSO4 + H2S
– Fe + CuSO4 = Cu + FeSO4
– СаО + СO2 = СаСО3
12. С каким соединением вступает в реакцию оксид углерода (IV)?
– H2O
– CaO
– C
+ Ca(OH)2
13. К экзотермическим относится реакция:
– электролиза воды
– дегидрирования этана
– разложения KMnO₄
+ нейтрализации H2SO4 гидроксидом калия
14. Гидролизу подвергается:
– BaSO₄
+ сахароза
– KBr
– глюкоза
15. Увеличение скорости реакции происходит с увеличением:
+ концентрации реагентов
– объёма продуктов реакции
– концентрации продуктов реакции
– объёма реагентов
16. Процесс разложения какого соединения является окислительно-восстановительной реакцией?
– NaHCO3
– малахита Cu₂(CO₃)(OH)₂
+ Zn(NO₃)₂
– (NH₄)₂CO₃
17. Какая реакция может служить примером реакции соединения?
+ S + O2 = SO2
– Al2O3 + 6HCl = 2AlCl3 + 3H2O
– Na + HCl = NaCl + H2
– BaCl2 + Na2SO4 = BaSO4 + NaCl
18. Какой металл не может вступать в реакцию замещения с серной кислотой?
– Cu
– Na
+ Mg
– Pb
19. Какая из реакций является окислительно-восстановительной и экзотермической?
+ 2Mg + O2 = 2MgO + Q
– N2 + O2 = 2NO – Q
– CaCO3 = CaO + CO2 – Q
– HCl + NaOH = NaCl + H2O + Q
тест-20. Как изменится скорость химического взаимодействия А + 2В = С, если температура повысится на 10 градусов (температурный коэффициент равен 2)?
+ увеличится 2 раза
– снизится в 4 раза
– увеличится в 3 раза
– снизится в 2 раза
21. Укажите тип химической реакции, изображённой на рисунке:
![]()
– обмена
– нейтрализации
– распада
+ соединения
22. В каком случае при понижении давления скорость реакции Fe (тв.) + H2SO4 (р-р) = FeSO4 (р-р) + Н2 (г) + Q повысится?
– при уменьшении температуры
+ при измельчении железа
– при разбавлении раствора кислоты
– при понижении концентрации серной кислоты
23. При нагревании Cu(OH)2 происходит реакция:
– соединения
– замещения
+ разложения
– обмена
24. К реакциям гидролиза не относится:
– K2SiO3 + H2O →
– CH3COOCH3 + NaOH(р-р) →
+ Na2O + H2O →
– Al4C3 + H2O →
25. Какой признак реакции между NaCl и AgNO3?
– выделение кислорода
+ выпадение осадка
– выделение газа
– образование воды
26. Взаимодействие CaCO3 + CO2 + H2O = Ca(HCO3)2 относится к реакциям:
– обмена
– замещения
– распада
+ соединения
27. Насколько достоверны представленные ниже суждения?
А. Скорость химического взаимодействия – это изменение концентрации реагентов за единицу времени.
Б. Концентрация компонента в смеси – это отношение массы компонента к объёму смеси.
+ достоверно лишь утверждение А
– достоверно лишь утверждение Б
– достоверны оба суждения
– оба суждения недостоверны
28. Уравнение 2КMnO4 = K2MnO4 + MnO2 + O2 описывает реакцию:
– обмена
– замещения
+ распада
– соединения
тест_29. Какой металл не реагирует с Cr2O3?
– медь
+ алюминий
– натрий
– все ответы верные

