Тесты по химии 9 класс. Тема: “Серная кислота и ее соли”
Правильный вариант ответа отмечен знаком +
1. На каком этапе добычи H2SO4 из пирита используется принцип противотока?
+ обжиг пирита
– получение олеума
– осушка SO₂
– все ответы верные
2. Анион SO42- даёт осадок с катионом:
– аргентума
– натрия
– калия
+ бария
3. Источниками сырья в производстве H2SO4 являются:
– самородная сера
– серный колчедан
– сульфиды цветных металлов CuS, Cu₂S, ZnS
+ все ответы верные
4. Какое из утверждений верное?
А) Процесс обжига серного колчедана – эндотермическая реакция.
Б) На этапе обжига FeS2 при повышении температуры более 800 °С скорость его обжига уменьшается, т. к. происходит спекание частичек пирита.
– верно лишь утверждение А
– верны оба утверждения
+ верно лишь утверждение Б
– неверны оба утверждения
5. Для поглощения SO3 используется:
– разбавленная серная кислота
– хлорид кальция
– оксид фосфора
+ концентрированная серная кислота
6. С какими соединениями реагирует H2SO4 (разб.)?
+ KOH,CuO, Zn
– SiO2, Cu, Fe
– K2O, Zn, Ag
– HBr, O2, SiO2
7. На каком этапе производства H2SO4 из пирита используется катализатор V₂O₅?
+ на I этапе
– на II этапе
– на III этапе
– на всех трёх этапах
8. Какая из солей серной кислоты является удобрением?
– MgSO4
+ K2SO4
– FeSO4
– Al2(SO4)3
9. Серная кислота окисляет HBr и HI до:
– хлорид-ионов
– простых металлов
+ свободных галогенов
– все ответы верные
тест 10. Осадок, который выпадает в ходе качественной химической реакции на серную кислоту и её соли:
– цветной кристаллический, не подвергается гидролизу
+ бесцветные кристаллы, не растворимые в воде и концентрированных кислотах
– легко растворяется в любых жидкостях
– нет правильного ответа
11.Продуктами обжига пирита (FeS2) являются:
– FeO и SO2
– FeO и SO3
+ Fe2O3 и SO2
– Fe2O3 и SO3
12. Не является сырьём в производстве H2SO4:
+ CS2
– FeS2
– H2S
– S
13. Какой процесс в производстве серной кислоты осуществляется в контактном аппарате?
– обжиг колчедана
– поглощение SO3 концентрированной H2SO4
+ окисление SO2 до SO3
– разбавление олеума
14. Какая реакция не характерна для производства серной кислоты?
– H2S + O2 → SO2 + Н2O
– S + O2 → SO2
– FeS2 + O2 → SO2 + Fe2O3
+ CS2 + O2 → SO2 + CO2
15. Как называются кислые соли серной кислоты?
– сульфаты
+ гидросульфаты
– cульфиты
– сульфиды
16. Концентрированная серная кислота является:
– сильным восстановителем
+ сильным окислителем
– одновременно и окислителем, и восстановителем
– нет верного ответа
17. Где не используется серная кислота?
– производство химических волокон
– производство минеральных удобрений
– производство взрывчатых веществ
+ производство виноматериалов
18. Сульфаты разлагаются:
– при низких температурах
+ при высоких температурах
– при любых температурах
– при комнатной температуре
19. Соли серной кислоты имеют все свойства:
– кислот
– оснований
+ солей
– активных металлов
тест-20. Укажите формулу сульфата натрия:
+ Na2SO4
– FeSO4
– CaSO4
– ZnSO4
21.Сульфаты переходных металлов разлагаются при температуре:
– 400-500 °С
– 800-1000 °С
– 1000-1200 °С
+ 700-800 °С
22. Выберите соль серной кислоты:
+ сульфат меди (II)
– сульфид меди (II)
– сульфит меди (II)
– силикат меди (II)
23. Выберите химическую формулу и изображение «глауберовой соли»:

24. Сфера применения железного купороса:
– обработка деревянных конструкций от грибков и плесени
– борьба с сельскохозяйственными вредителями
– профилактика хлороза
+ все ответы верные
25. Чем опасно разбавление концентрированной серной кислоты приливанием к ней воды?
– возникновением пожара
– разложением воды
– выделением ядовитого вещества
+ разбрызгиванием раствора вследствие выделения теплоты
26. Объясните понятие термина «купоросы»:
– средние соли серной кислоты
+ некоторые гидратированные сульфаты
– кислые соли серной кислоты
– все ответы верные
27. Вставьте пропущенные слова: «Серная кислота и её соли осаждают катионы …, в результате чего выпадает …:
+ Pb2+, белый осадок PbSO4
– Zn2+, бурый осадок ZnSO4
– Ва2+, жёлтый осадок BaSO4
– Cu2+, синий осадок CuSO4
28. Каким уравнением описывается качественная реакция на сульфат-ион?
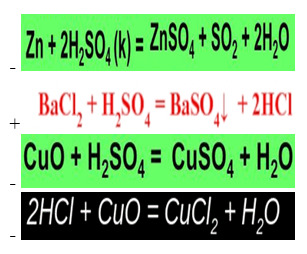
29. Какое из свойств не относится к серной кислоте:
– проявляет общекислотные свойства
– образовывает белый мелкокристаллический осадок с нитратом бария
– реагирует с металлами, стоящими в ряду напряжений после водорода, неметаллами
+ кислота средней силы
тест_30. Серная кислота имеет … класс опасности.
– III
– I
+ II
– IV

